Kamakura đồng hành kết nối bệnh nhân với các trung tâm y khoa tiên tiến, mở ra cơ hội tiếp cận liệu pháp CAR-T trong điều trị ung thư.
-
CAR T-Cell Therapy là một liệu pháp miễn dịch (immunotherapy) dùng để điều trị một số loại ung thư máu.
-
Trong liệu pháp này, các tế bào T của bạn (một loại tế bào miễn dịch) được lấy ra, sửa đổi trong phòng thí nghiệm bằng cách thêm vào một gene nhân tạo gọi là chimeric antigen receptor (CAR). Gene này giúp tế bào T có khả năng nhận biết và tiêu diệt các tế bào ung thư hiệu quả hơn.
-
CAR T-cell đôi khi được gọi là “thuốc sống” (living drug) vì khi được truyền lại vào cơ thể, chúng có thể nhân lên, hoạt động dài lâu để kiểm soát ung thư.
Những loại ung thư nào được điều trị bằng CAR T?
Liệu pháp này thường được dùng khi các phương pháp khác không hiệu quả hoặc ung thư tái phát. Các loại ung thư máu được áp dụng hiện nay gồm:
-
B-cell acute lymphoblastic leukemia (ALL)
-
Diffuse large B-cell lymphoma
-
Follicular lymphoma
-
Mantle cell lymphoma
-
Multiple myeloma
-
Và các lymphoma B-cell cấp cao khác
Ngoài ra, CAR T đang đươc nghiên cứu thử nghiệm lâm sàng trên khối u rắn. Dưới đây là các thông tin cập nhật về thử nghiệm lâm sàng CAR-T trên u rắn (solid tumors), kèm những thách thức & hướng phát triển được quan tâm hiện nay.
Những thử nghiệm CAR-T trên u rắn/ ung thư thể đặc (solid tumors)
| Tên Thử Nghiệm | Loại U rắn (thể đặc)/ chỉ định | Giai đoạn & Kết quả sơ bộ |
|---|---|---|
|
ALLO-316(CAR T allogeneic nhắm mục tiêu CD70) |
Thận (clear cell renal cell carcinoma, ccRCC) |
Giai đoạn I, thử nghiệm “TRAVERSE” tại MD Anderson ‒ bệnh nhân đã thất bại với các liệu pháp ức chế điểm kiểm soát miễn dịch (checkpoint inhibitors) và chất ức chế tyrosine kinase. ORR ~ 18%, DCR ~ 82%. Với nhóm có biểu hiện CD70 dương đặc biệt, ORR tăng lên ~ 33%, DCR ~ 100%. |
|
CTX130™ |
Cũng là ccRCC (thận) |
Thử nghiệm “COBALT-RCC” ‒ allogeneic CAR-T “off-the-shelf” (có sẵn) cho u thận kháng trị. Khoảng 81% bệnh nhân có ích lợi lâm sàng (clinical benefit): phần lớn là ổn định bệnh (stable disease), có ít nhất một trường hợp đáp ứng hoàn toàn (complete response) kéo dài > 3 năm. |
|
IVS-3001 |
Các u rắn có biểu hiện HLA-G dương (clear cell RCC, ung thư buồng trứng biểu mô, và các loại u HLA-G dương khác) |
Giai đoạn I/IIa, thử nghiệm mở (open label), kết hợp MD Anderson & Invectys & CTMC. Dự kiến hoàn thành vào khoảng năm 2029. |
|
AIC100 nhắm ICAM-1 |
Ung thư tuyến giáp tiên tiến (hai phân nhóm ung thư tuyến giáp ác tính) |
Giai đoạn I, thử nghiệm “first-in-human” tại MD Anderson. Có đáp ứng khuyến khích và hồ sơ an toàn chấp nhận được. Một bệnh nhân có đáp ứng hoàn toàn. |
Thách thức trong CAR-T u rắn
Dù có những tiến bộ, có nhiều khó khăn mà CAR-T vẫn chưa vượt qua được trong u rắn:
-
Sự khác biệt và không đồng nhất của biểu hiện antigen
-
U rắn thường có biểu hiện mục tiêu (target antigen) không đều giữa các tế bào trong cùng một khối u, hoặc giữa bệnh nhân này với bệnh nhân khác. Nếu CAR-T nhắm vào antigen đó mà một phần tế bào không có, khối u có thể “né tránh” bằng cách nhóm tế bào không có antigen đó.
-
-
Thâm nhập vào khối u & môi trường khối u ức chế miễn dịch (TME: tumor microenvironment)
-
Các tế bào T cần phải tới được bên trong khối u, vượt qua mạch máu, mô kẽ, hàng rào vật lý (stroma), và hàng rào hóa học/miễn dịch (ví dụ cytokine ức chế, tế bào ức chế như MDSC - myeloid-derived suppressor cells).
-
Tế bào CAR-T trong u rắn thường bị “kiệt sức” (exhaustion), không tồn tại lâu, hoặc bị ức chế bởi các tín hiệu tiêu cực.
-
-
Tính an toàn và tác dụng phụ
-
Rủi ro như độc tính, phản ứng quá mức miễn dịch, có thể nguy hiểm hơn khi CAR-T hoạt động trong mô rắn với khối u lớn hoặc lan rộng.
-
Thiếu mục tiêu “an toàn” đặc hiệu, vì nhiều antigen cũng có biểu hiện ở mô lành gây nguy cơ tấn công tế bào lành.
-
-
Sản xuất & chi phí
-
Allogeneic (sẵn có) so với autologous (lấy từ chính bệnh nhân) có lợi ích về thời gian, nhưng có vấn đề về tương hợp miễn dịch, khả năng bị nhận diện và loại bỏ.
-
Chi phí chế tạo cao, yêu cầu quy trình sản xuất nghiêm ngặt
-
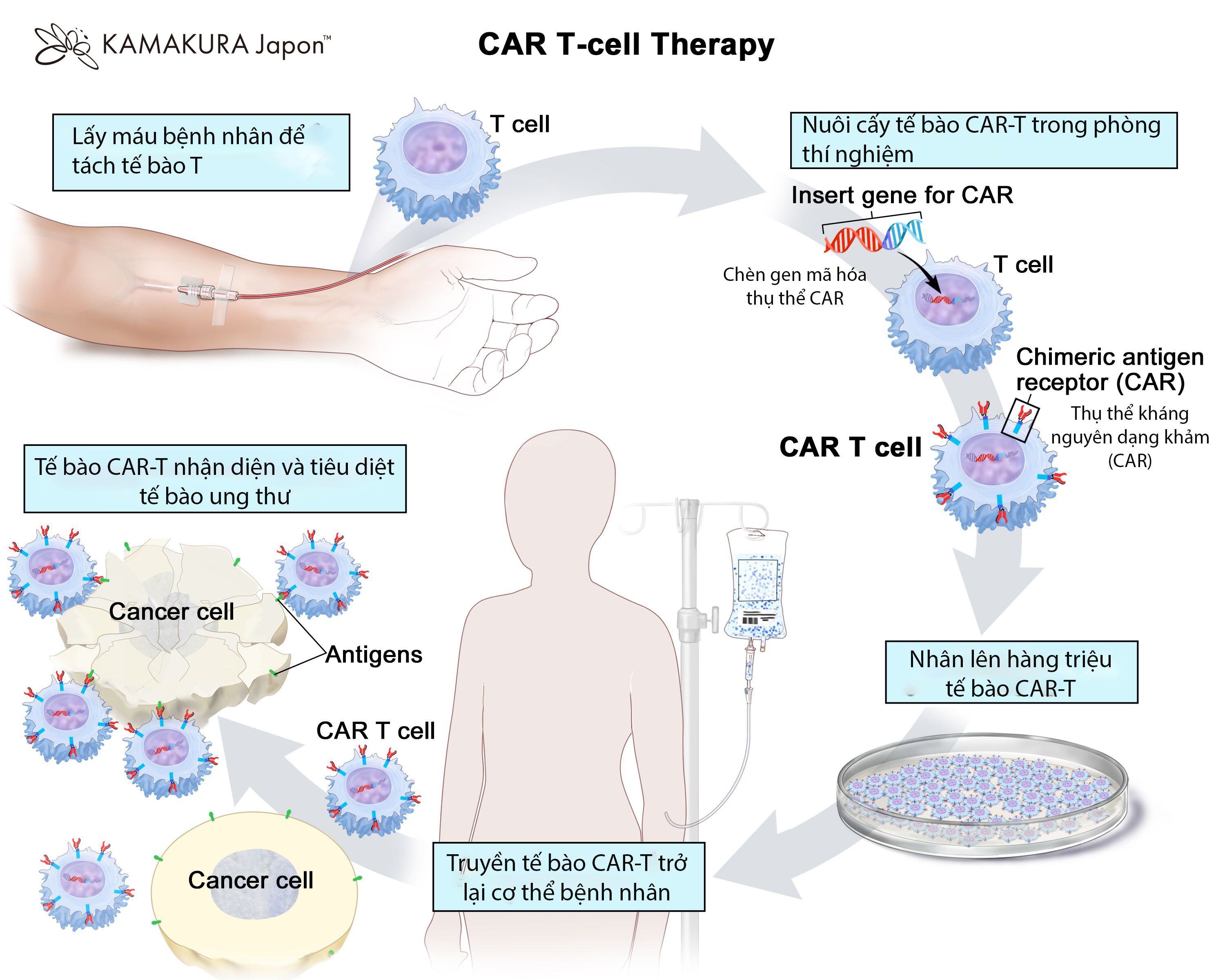
Quá trình điều trị diễn ra như thế nào?
-
Lấy tế bào T
-
Bằng cách dùng phương pháp gọi là leukapheresis: máy sẽ lấy máu của bạn, tách tế bào T ra, phần còn lại trả lại cơ thể.
-
-
Chỉnh sửa tế bào
-
Đưa gene CAR vào tế bào T trong phòng thí nghiệm. Tế bào T được biến đổi này có thể nhận diện kháng nguyên đặc trưng trên tế bào ung thư.
-
Sau đó các tế bào này được nhân lên để đủ số lượng cần thiết. Quá trình này có thể mất vài tuần (thường khoảng 3-6 tuần).
-
-
Chuẩn bị cơ thể
-
Trước khi truyền lại tế bào CAR T, bệnh nhân có thể được hóa trị hoặc bức xạ nhẹ (bridging therapy) để giảm tải ung thư trong thời gian tế bào CAR T được sản xuất.
-
Còn có bước dùng hóa trị làm giảm lymphocyte (lymphodepleting chemotherapy) để “dọn đường”, giúp cơ thể chấp nhận CAR T tốt hơn.
-
-
Truyền tế bào CAR T
-
Khi tế bào đã sẵn sàng, chúng được truyền vào cơ thể bằng đường truyền tĩnh mạch (IV infusion) — quá trình khá nhanh (khoảng vài phút đến vài chục phút) giống truyền máu.
-
-
Theo dõi sau điều trị
-
Sau truyền, bệnh nhân thường được nằm viện để theo dõi tác dụng phụ, vì có thể xảy ra những phản ứng nặng.
-
Trong tháng đầu sau điều trị, cần gần cơ sở y tế để bất cứ dấu hiệu bất thường nào cũng có thể xử lý nhanh.
-
Những rủi ro / tác dụng phụ
-
Cytokine release syndrome (CRS) — hội chứng “giải phóng cytokine”: gây ra sốt, khó thở, huyết áp thấp, thậm chí suy đa tạng nếu nghiêm trọng.
-
Vấn đề thần kinh: có thể gặp như khó nói, lú lẫn, co giật, thay đổi thị giác, tremor, vân vân.
-
Các tác dụng phụ khác: mệt mỏi, dễ chảy máu, tăng nguy cơ nhiễm trùng, thay đổi điện giải (ví dụ kali, natri thấp), và phản ứng dị ứng trong khi truyền tế bào.
Lợi ích & hiệu quả
-
Cho nhiều người khi các phương pháp trước đó không thành công, CAR T-cell therapy có thể mang lại thuyên giảm hoàn toàn (remission). Ví dụ: trong một nghiên cứu năm 2020 với trẻ em bị ALL, hơn 85% đạt thuyên giảm ngay sau điều trị; trong số này khoảng 60% vẫn giữ trạng thái không có ung thư sau 12 tháng.
-
Đối với vài trường hợp, liệu pháp này thậm chí có thể chữa được (cure) hoặc kéo dài cuộc sống đáng kể hơn so với các lựa chọn khác.
Tham khảo chi phí CAR-T trên thế giới
|
Khu vực / Quốc gia |
Chi phí trung bình / khoảng |
Ghi chú & thành phần chi phí |
|
Mỹ |
Khoảng US$ 373.000 ‒ US$ 475.000chỉ riêng chi phí thuốc / sản phẩm CAR-T. |
Không bao gồm các chi phí điều trị phụ trợ (như hóa trị trước, chăm sóc đặc biệt nếu có CRS, điều trị biến chứng, nhập viện dài ngày, xét nghiệm, v.v.). Khi tính hết, tổng chi phí có thể lên tới US$ 700.000 đến trên $1.000.000 trong một số trường hợp. |
|
Châu Âu |
Khoảng €300.000 ‒ €350.000(khoảng US$ 320.000-400.000 tùy tỷ giá) cho một liệu trình CAR-T tiêu chuẩn. |
Đây là giá niêm yết / giá của các sản phẩm thương mại. Có nước hoặc trung tâm “sản xuất nội bộ” (in-house) có thể rẻ hơn nhiều — ví dụ ở Tây Ban Nha phát triển CAR-T công lập được báo là ~ €90.000. |
|
Trung Quốc |
Phạm vi rộng: khoảng US$ 55.000 ‒ ~ US$ 350.000 tùy loại, địa điểm, sản phẩm. |
Giá thấp hơn khi sản phẩm được sản xuất trong nước, hỗ trợ chính phủ, hoặc chi phí y tế/nội trú thấp hơn. |
|
Ấn Độ |
Khoảng US$ 45.000 ‒ US$ 75.000cho các loại CAR-T trong nước, đặc biệt sản phẩm “nội địa” (Made-in-India). |
Chi phí phụ thuộc vào loại CAR-T, mức độ chăm sóc bệnh nhân, liệu có phải nhập khẩu hay sản xuất trong nước, nếu phải ICU, biến chứng,… |
|
Singapore |
US$ 375.000 – 475.000 (~ S$480.000 – 620.000) |
Có trợ cấp CTGTP: Công dân SG được hỗ trợ tới 75% (tối đa S$150.000); PR ~22,5% (tối đa S$45.000) |
|
Malaysia |
Ước tính từ khoảng US$ 200.000 đến ~ US$ 400.000 cho bệnh nhân quốc tế. |
Bao gồm chi phí toàn bộ liệu trình (thu thập tế bào, chế tạo, hóa trị chuẩn bị, truyền, theo dõi sau) nhưng vẫn có thể có thêm chi phí phát sinh tùy tình trạng bệnh. |
|
Thái Lan |
Khoảng US$ 150.000 ‒ US$ 470.000tùy thành phố, bệnh viện. |
Chi phí dao động lớn tùy hạ tầng, mức độ cần chăm sóc đặc biệt, loại CAR-T. |
Những yếu tố ảnh hưởng mạnh tới chi phí
-
Giá thuốc CAR-T (gene-modified T cell) / sản phẩm chính của công ty dược.
-
Chi phí thu thập tế bào (apheresis), hóa trị chuẩn bị (lymphodepleting), xét nghiệm chuẩn đoán, genotyping.
-
Chi phí bệnh viện: ngày nằm viện, ICU nếu có biến chứng nặng (ví dụ CRS), chăm sóc sau truyền.
-
Chi phí quản lý biến chứng, theo dõi dài hạn.
-
Nếu sản phẩm “in-house” hoặc sản xuất địa phương vs nhập khẩu.
-
Chính sách bảo hiểm / hỗ trợ tài chính của quốc gia.